APPROFONDIMENTI
Opicapone: una nuova opzione per i pazienti con malattia di Parkinson, ora disponibile anche in Italia
Redazione OnMedicine

Opicapone è un inibitore della Catecol-O-MetilTransferasi (COMT) di terza generazione e, al momento, è l’unica molecola della sua classe ad aver ricevuto l’approvazione dell’EMA;1 è attualmente disponibile nel Regno Unito, in Spagna e in Germania per il trattamento aggiuntivo a levodopa/inibitori della DOPA-decarbossilasi in soggetti adulti affetti da Malattia di Parkinson con fluttuazioni di fine dose non stabilizzate da queste combinazioni terapeutiche;2 da settembre questa molecola è disponibile anche in Italia al dosaggio di 50 mg.
Opicapone è stato sviluppato per fornire un’elevata azione inibitoria sull’enzima COMT, evitando nel contempo lo sviluppo di tossicità epatica, tipico evento avverso correlato a questa classe di farmaci.3
L’inibizione dell’enzima COMT generata da questa molecola è più potente e di durata maggiore rispetto ad altre molecole con meccanismo d’azione paragonabile, come entacapone e tolcapone. La lenta cinetica di reazione legame-ligando consente infatti un prolungamento della sua durata d’azione fino a 24 ore, rendendolo adatto a una singola somministrazione giornaliera.2
L’iter di approvazione
L’approvazione del farmaco si è basata sui risultati di due studi di fase III: il BIA-91067-301 (BIPARK-I)4 e il BIA-91067-302 (BIPARK-II), entrambi condotti in doppio cieco, controllati vs placebo e, solo per il primo studio, con controllo attivo (entacapone).3,4
Nel BIPARK-I inoltre, i pazienti sono stati randomizzati a ricevere tre diversi dosaggi di opicapone (5, 25 e 50 mg), mentre nel BIPARK-II sono stati testati solo i due dosaggi più elevati.4
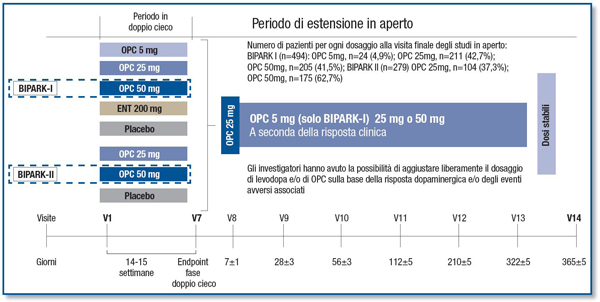
La durata della fase in doppio cieco è stata di 15 settimane, alla fine della quale i soggetti inclusi sono stati invitati a entrare nella fase di estensione, in aperto, della durata di un anno, dove a tutti i partecipanti, indipendentemente dal trattamento ricevuto nella fase in doppio cieco, è stato somministrato, per la prima settimana, opicapone 25 mg (Figura 1). Il dosaggio del farmaco poteva in seguito essere modulato sulla base della risposta clinica, aumentandolo fino al dosaggio attualmente in commercio di 50 mg.3
L’endpoint primario di questi due studi era la variazione, in termini di tempo, della fase OFF.
Lo studio BIPARK-I ha documentato una riduzione media di questo parametro di due ore con l’utilizzo di opicapone 50 mg, dato statisticamente significativo rispetto a placebo e non inferiore rispetto a entacapone.4
Il dato versus placebo è stato confermato anche nel BIPARK-II.
L’analisi combinata dei due studi, perfettamente confrontabili sulla base degli endpoint e del disegno dello studio, ha confermato i risultati ottenuti dai due studi considerati individualmente.3
Tra gli endpoint secondari di maggiore interesse è stata valutata la proporzione di OFF-time responders, definita come la percentuale di pazienti con una riduzione della fase OFF di almeno 1 ora a seguito del trattamento. Nei pazienti in terapia con opicapone 25 e 50 mg questo parametro è risultato significativamente maggiore rispetto a placebo in entrambi gli studi e anche nell’analisi combinata. Nei pazienti trattati con entacapone, invece, la proporzione è risultata paragonabile al placebo.3
Un altro outcome clinico interessante considerato è stata la variazione del tempo in fase ON in assenza di discinesia rilevante: la terapia con opicapone 50 mg ha ottenuto la significatività statistica. Il BIPARK-II ha confermato il trend, senza però raggiungere la significatività statistica, confermata invece nell’analisi combinata.3
Durante questi studi è stata inoltre richiesta ai pazienti una valutazione globale della terapia: è risultato che i pazienti che si consideravano “molto migliorati” erano in numero maggiore nel braccio in trattamento con opicapone.3
L’analisi condotta ha confermato il buon profilo di sicurezza del farmaco: l’incidenza di eventi avversi che ha portato a interruzione del trattamento registrata nei pazienti in terapia con opicapone è risultata sovrapponibile al placebo. L’evento avverso più frequente è stato, come atteso, la discinesia: l’insorgenza di questo disturbo non ha però influito sul numero di interruzioni del trattamento: non è emersa dunque nessuna particolare segnalazione inattesa in termini di sicurezza del farmaco.3
Fase di estensione
I risultati della fase di estensione in aperto hanno dimostrato il mantenimento dell’effetto ottenuto nella fase in doppio cieco e i pazienti passati da entacapone a opicapone hanno ottenuto, dopo un anno, un’ulteriore riduzione della fase OFF di 0,7 ore.3 Con tutti i limiti da considerare riguardo al fatto che si tratta di uno studio in aperto è però possibile concludere che i pazienti che passano a opicapone da altre terapie ottengono un guadagno in termini di riduzione della fase OFF. Il periodo di estensione dello studio, inoltre, ha confermato la sicurezza della terapia: l’evento avverso più comune si è confermato la discinesia e la frequenza di diarrea, nausea e discolorazione delle urine è inoltre risultata inferiore rispetto a entacapone. Non sono stati registrati infine casi gravi di epatotossicità.3
Conclusioni
Opicapone dunque, grazie al suo favorevole profilo farmacocinetico e farmacodinamico, insieme alla praticità di somministrazione (una volta al giorno) e alla sua buona tollerabilità può essere considerato una nuova e valida opzione di trattamento per la Malattia di Parkinson.3,5
Sintesi ragionata della presentazione omonima a cura di
Joaquim Ferreira
Laboratorio di Farmacologia Clinica e Terapeutica, Facoltà di Medicina, Università di Lisbona CNS Campus Neurológico Sénior
Roma, 25 maggio 2018
Il report integrale del simposio è stato pubblicato a Luglio come supplemento On Medicine3
Bibliografia
- http://www.ema.europa.eu/ema/index.jsp?curl=pages/medicines/human/medicines/002790/human_med_001950.jsp&mid=WC0b01ac058001d124
- RCP Ongentys®
- “Opicapone: una nuova opzione per i pazienti con malattia di Parkinson." On Medicine Anno XIII, Suppl. al n. 2, 2018.
- Ferreira J et al. The Lancet Neu¬rology 2015;15(2):154-65
- Scott LJ. Drugs 2016;76:1293-300
-
Farmacologia clinica dei farmaci anticoagulanti
Marco Moia Centro Emofilia e Trombosi - Fondazione IRCCS Ca’ Granda Ospedale Maggiore Policlinico di Milano
-
Sintomi del basso apparato urinario dopo chirurgia pelvica: fisiopatologia e trattamento
Enrico Finazzi Agrò - Professore Associato; Cattedra di Urologia, Università di Roma “Tor Vergata”; UOSD Servizio di Urologia Funzionale, Policlinico Tor Vergata; IRCCS Ospedale S. Lucia, Roma
-
Fisiologia di apprendimento e memoria
Mariano Pedetti - SerT MVT, AUSL2 dell‘Umbria, Marsciano (PG)